2018ЯТАыФъГѕжаЛЏбЇНЬЪІзЪИёжЄУцЪдПМЬтЃЈОЋбЁЃЉЕкЫФХњ
ЗЂВМЪБМфЃК2019-04-12 11:15:10 БрМЉЃКЪІДѓДДГЬНЬг§
ГѕжаЛЏбЇЁЖШмвКЕФХфжЦЁЗ
вЛЁЂПМЬтЛиЙЫ

 ЖўЁЂПМЬтНтЮі
ЖўЁЂПМЬтНтЮі
ЁОНЬбЇЙ§ГЬЁП
(вЛ)ЬИЛАЕМШы
ЁОНЬЪІЬсЮЪЁПЩЯНкПЮЮвУЧСЫНтСЫШмвКЁЂШмжЪЁЂШмМСЕШетаЉИХФюЃЌРЯЪІетРягавЛБбЮЫЎЃЌЫФмРДИјРЯЪІЫЕвЛЯТбЮЫЎжаЕФШмжЪЁЂШмМСЗжБ№ЪЧЪВУД?
ЁОбЇЩњЛиД№ЁПбЮЫЎжаЃЌТШЛЏФЦЪЧШмжЪЃЌЫЎЪЧШмМСЃЌбЮЫЎЮЊШмвК
ЁОНЬЪІзмНсЁПФЧШчЙћРЯЪІИцЫпДѓМветБбЮЫЎжаТШЛЏФЦЕФжЪСПЗжЪ§ЪЧ10%ЃЌзмжЪСПЪЧ80gЕФЛАЃЌШчКЮзМШЗЕФХфжЦетбљвЛБШмвКФи?
(Жў)аТПЮНЬбЇ
1.ЪЕбщЧАзМБИ
ЁОНЬЪІЬсЮЪЁПШчЙћЯывЊХфжЦвЛЖЈжЪСПЗжЪ§ЕФШмвКЃЌДѓМвВТЯывЛЯТЃЌЮвУЧашвЊзМБИФФаЉЪЕбщгУЦЗвдМАЪЕбщЦїВФФи?
ЁОбЇЩњЛиД№ЁПашвЊЭаХЬЬьЦНГЦШЁШмжЪЕФжЪСП
ЁОбЇЩњЛиД№ЁПВЃСЇАєНјааНСАшЃЌЩеБНјааЪЂзАвКЬхЁЃ
ЁОбЇЩњЛиД№ЁПвЉЦЗТШЛЏФЦЁЂеєСѓЫЎ
ЁОНЬЪІзмНсЁПДѓМвзмНсЕФЖМКмКУЃЌашвЊзМБИЕФЪЕбщЦїВФАќРЈЃЌЭаХЬЬьЦН(ЛђЕчзгГг)ЁЂЩеБЁЂВЃСЇАєЁЂТШЛЏФЦвдМАеєСѓЫЎЃЌСПЭВЁЂдПГзЁЃ
ЁОНЬЪІЬсЮЪЁПЭЌбЇУЧЃЌдкЪЙгУжЎЧАЃЌЯШЛиЙЫвЛЯТЭаХЬЬьЦНЕФЪЙгУВНжш
ЁОбЇЩњЛиД№ЁП(1)зѓЮягвэР;(2)ЪЙгУЧАЕїНкЦНКтЃЌЕїНкгЮТыЁЂжИеыЖМЙщСу;(3)ШЁгУэРТыгУФїзг;(4)ЮяЦЗВЛФмжБНгЗХдкЭаХЬЩЯГЦСПЃЌашвЊЗХдкжНЩЯЛђепЩеБжа;(5)ГЦСПЭъБЯНЋэРТыЗХШыКаФкЃЌНЋгЮТыЙщСуЁЃ
2.ЖЏЪжЪЕбщ
ЁОНЬЪІЬсЮЪЁПдкзіЪЕбщжЎЧАЮвУЧгІИУзіФФаЉзМБИ?
ЁОбЇЩњЛиД№ЁПашвЊЯШМЦЫуГіЫљвЊГЦШЁЕФТШЛЏФЦЕФжЪСПЃЌвВОЭЪЧ80g×10%=8g
ЁОНЬЪІв§ЕМЁПЯждкЭЌбЇУЧПЩвдвдЪЕбщаЁзщЮЊЕЅЮЛЃЌРДЩшМЦвЛЯТХфжЦ80g 10%ТШЛЏФЦШмвКЕФСїГЬМАВНжш
ЁОбЇЩњЛиД№ЁП(1)ШЁТШЛЏФЦвЉЦЗ(МЦЫу);(2)ГЦСП;(3)ШмНт
ЁОНЬЪІв§ЕМЁПФЧЭЌбЇУЧИљОнФуУЧЩшМЦЕФЪЕбщЗНАИПЊЪМЖЏЪжзіЪЕбщЃЌдкЪЕбщЕФЙ§ГЬжазЂвтЪЕбщВйзїЕФЙцЗЖадвдМАаЁзщжЎМфЕФКЯзїЗжХфЁЃ
ЁОНЬЪІЬсЮЪЁПЭЌбЇУЧЫЕвЛЯТдкСПШЁеєСѓЫЎвдМАНСАшжазЂвтЕФЪТЯю?
ЁОбЇЩњЛиД№ЁПБОДЮЪЕбщЫљашеєСѓЫЎЪЧ72mLЃЌЯШгУ100mLСПЭВСПШЁ70mLеєСѓЫЎЃЌЦфДЮдйгУ10mLСПШЁ2mLеєСѓЫЎЃЌдкСПШЁжавЊзЂвтНЋСПЭВЗХЦНЃЌЪгЯпгыПЬЖШЯпБЃГжЫЎЦН;НСАшЙ§ГЬжавЊБпМгЫЎБпНСАшЃЌЖјЧвНСАшЪБКђОЁСПВЛвЊЪЙВЃСЇАєДЅХіШнЦїЕФЦїБкЁЃ
ЁОНЬЪІзмНсЁПЭЌбЇУЧдкИеИеЕФЪЕбщжаВйзїЖМКмЙцЗЖЁЃдкХфжЦвЛЖЈжЪСПЗжЪ§ЕФШмвКЕФЪЕбщжаЃЌЕквЛВНЪЧМЦЫуШмжЪЁЂШмМСЕФжЪСП;ЕкЖўВНЪЧГЦСПвЉЦЗ;ЕкШ§ВНЪЧМгЫЎНСАшШмНтЁЃ
(Ш§)ЙЎЙЬЬсИп
ЁОНЬЪІЬсЮЪЁП
(1)ГЦСПЪБЃЌвЉЦЗКЭэРТыЗХЗДСЫЃЌЕЋЪЧУЛгаЪЙгУгЮТыЃЌЖдНсЙћЕФгАЯьЪЧЪВУД?
(2)ВЃСЇАєЕФзїгУЪЧЪВУД?
(3)дкСПШЁШмМСЪБЃЌИЉЪгСПЭВЃЌдьГЩНсЙћЦЋДѓЛЙЪЧЦЋаЁ?
(ЫФ)аЁНсзївЕ
аЁНсЃКбЇЩњзмНсБОНкПЮжиЕужЊЪЖЃЌНЬЪІВЙГфЁЃ
зївЕЃКгыЭЌбЇМфНЛСїБОДЮЪЕбщЕФОбщКЭНЬбЕЁЃ
ЁОАхЪщЩшМЦЁП

ЁОД№БчЬтФПНтЮіЁП
1.ШчЙћдкЪЕбщВйзїжаЃЌдкГЦСПвЉЦЗЙ§ГЬжаЃЌЗЂЯжЕцжНвдКѓЃЌЬьЦНжИеыЯђзѓЦЋЃЌНсЙћЛсдѕбљ?
ЁОВЮПМД№АИЁП
жЛдкГЦСПЪГбЮЕФЭаХЬЕцЩЯСЫИЩОЛЕФжНЃЌЕМжТГЦСПЕФЪГбЮжЪСПЦЋЕЭЃЌШмжЪжЪСПЗжЪ§ЦЋЕЭЁЃ
2.НЋСПЭВжаЕФЫЎЕЙШыЩеБЪБЃЌЩеБжагаЩйСПЫЎВагрЃЌЪЕбщНсЙћЛсдѕбљ?
ЁОВЮПМД№АИЁП
НЋСПЭВжаЕФЫЎЕЙШыЩеБЪБЃЌвђЮЊСПЭВжагаЩйСПЫЎВагрЃЌЪЙЫљХфТШЛЏФЦШмвКжаЕФЫЎМѕЩйСЫЃЌжЪСПЗжЪ§БфДѓСЫЁЃ
2018ФъЯТАыФъНЬЪІзЪИёУцЪд-ЛЏбЇбЇПЦ-ЪдНВМАД№Бч-ПМЬтНтЮі
ГѕжаЛЏбЇЁЖЙЬЬхвЉЦЗЕФШЁгУЁЗ
вЛЁЂПМЬтЛиЙЫ
 ЖўЁЂПМЬтНтЮі
ЖўЁЂПМЬтНтЮі
ЁОНЬбЇЙ§ГЬЁП
(вЛ)ИДЯАЕМШы
ЁОЬсГіЮЪЬтЁПЧАМИНкПЮЮвУЧбЇЯАСЫЪЕбщвЧЦїЕФУћГЦЁЂЬиЕуЁЂгУЭОвдМАЪЕбщЪвАВШЋЙцдђ?ФЧЪЕбщЪвАВШЋддђЖМгаФФаЉ?
ЁОбЇЩњЛиД№ЁПЂйВЛФмгУЪжНгДЅвЉЦЗ;
ЂкзЂвтНкдМвЉЦЗЃЌгІИУбЯИёАДееЪЕбщЙцЖЈ;
ЂлЪЕбщЪЃгрЕФвЉЦЗВЛФмЗХЛидЦПЃЌвЊЗХШыжИЖЈЕФШнЦїжаЁЃ
ЁОНЬЪІв§ЕМЁПЮвУЧдкЪЕбщЪвзіЪЕбщЕФЪБКђРыВЛПЊОпЬхЕФЪЕбщВйзїЃЌЮвУЧетвЛНкОЭПЊЪМбЇЯАОпЬхЕФЪЕбщВйзїЃЌЪзЯШЮвУЧРДбЇЯАЙЬЬхвЉЦЗЕФШЁгУЁЃ
(Жў)ЬНОПаТжЊ
1.ПщзДЙЬЬхЛђН№ЪєПХСЃЕФШЁгУ
ЁОЖрУНЬхеЙЪОЁПШЁгУПщзДЙЬЬхвЉЦЗ(ЪЏЛвЪЏКЭН№ЪєаП)ЕФЪгЦЕЃЌбЇЩњЙлВьвЉЦЗЕФзДЬЌЁЂвЉЦЗДцЗХЪдМСЦПЕФЬиеїЁЂШЁгУвЉЦЗЕФвЧЦївдМАВйзїЫГађЁЃ
ЁОбЇЩњЛиД№ЁП
ЂйПщзДЙЬЬхвЉЦЗЭЈГЃБЃДцдкЙуПкЦПРяЃЌПЩгУФїзгМаШЁ;
ЂкгУЙ§ЕФФїзгвЊСЂПЬгУИЩОЛЕФжНВСЪУИЩОЛЃЌвдБИЯТДЮЪЙгУЁЃ
ЁОНЬЪІзмНсЁППщзДЙЬЬхвЉЦЗЕФШЁгУЕФвЧЦїЪЧФїзгЃЌВНжшЮЊвЛКсЖўЗХШ§Т§ЪњЁЃ
ЁОбнЪОВйзїЁПЪзЯШАбУмЖШНЯДѓЕФПщзДвЉЦЗЛђН№ЪєПХСЃЗХШыВЃСЇШнЦїЪБЃЌгІИУЯШАбШнЦїКсЗХЃЌАбвЉЦЗЛђН№ЪєПХСЃЗХШыШнЦїПквдКѓЃЌдйАбШнЦїТ§Т§ЕиЪњСЂЦ№РДЃЌЪЙвЉЦЗЛђН№ЪєПХСЃЛКЛКЕиЛЌЕНШнЦїЕФЕзВПЃЌвдУтДђЦЦШнЦїЁЃ
ЁОбЇЩњЪЕбщЁПЪЕбщ1-3ЃК(1)гУФїзгМаШЁЩйСППХСЃзДЪЏЛвЪЏ(ЛђДѓРэЪЏ)ЗХШыЪдЙмжаЃЌВЂНЋЪдЙмЗХдкЪдЙмМмЩЯБИгУЁЃ
ЁОНЬЪІбВЪгжИЕМЁПЧПЕїЪдЙмвЛЖЈвЊЛКТ§ЪњЦ№ЃЌЫйЖШВЛФмЬЋПьЁЃ
2.ЗлФЉзДЛђаЁПХСЃзДвЉЦЗЕФШЁгУ
ЁОУНЬхеЙЪОЁПШЁгУЗлФЉзДЙЬЬхвЉЦЗ(ЬМЫсФЦЗлФЉ)ЕФЪгЦЕЃЌбЇЩњЙлВьвЉЦЗЕФзДЬЌЁЂвЉЦЗДцЗХЪдМСЦПЕФЬиеїЁЂШЁгУвЉЦЗЕФвЧЦївдМАВйзїЫГађЁЃ
ЁОЪІЩњзмНсЁПЗлФЉзДЙЬЬхвЉЦЗЭЈГЃБЃДцдкЙуПкЦПРяЃЌПЩгУдПГзМаШЁЁЃгУЙ§ЕФдПГзвЊСЂПЬгУИЩОЛЕФжНВСЪУИЩОЛЃЌвдБИЯТДЮЪЙгУЁЃ
ЁОНЬЪІзмНсЁПЗлФЉзДвЉЦЗЕФШЁгУЕФвЧЦїЪЧдПГзЛђжНВлЃЌВНжшЮЊвЛКсЖўЫЭШ§жБСЂЁЃ
ЁОбнЪОВйзїЁПЭљЪдЙмРязАШыЙЬЬхЗлФЉЪБЃЌЮЊБмУтвЉЦЗеДдкЙмПкКЭЙмБкЩЯЃЌПЩЯШЪЙЪдЙмЧуаБЃЌАбЪЂгавЉЦЗЕФвЉГз(ЛђгУаЁжНЬѕелЕўГЩЕФжНВл)аЁаФЕиЫЭжСЪдЙмЕзВПЃЌШЛКѓЪЙЪдЙмжБСЂЦ№РДЁЃ
ЁОНЬЪІВЙГфЁПЙЬЬхвЉЦЗШЁгУддђЃКВЛДЅЃЌВЛЮХЃЌВЛГЂ;НкдМвЉЦЗ;гУЪЃЕФвЉЦЗЗХШыжИЖЈШнЦїЁЃ
(Ш§)ЭиеЙЬсЩ§
ЁОбЇЩњЪЕбщЁПЪЕбщ1-3ЃК(2)ШЁЩйСПЬМЫсФЦЗлФЉЗХШыСэвЛжЇЪдЙмжаЃЌВЂНЋЪдЙмЗХдкЪдЙмМмЩЯБИгУЁЃНЬЪІбВЪгжИЕМЁЃ
(ЫФ)аЁНсзївЕ
аЁНсЃКбЇЩњзмНсЙщФЩБОНкПЮЫљбЇжївЊжЊЪЖЃЌБэЪібЇЯАаФЕУЁЃ
зївЕЃКРћгУМвжаЕФБзгЁЂЦПзгЁЂЭыЁЂПъЁЂГзЕШЃЌвдМАЪГбЮЁЂБљЬЧНјааЙЬЬхвЉЦЗЕФШЁгУСЗЯАЁЃ
ЁОАхЪщЩшМЦЁП
ЁОД№БчЬтФПНтЮіЁП
1.ИјЪдЙмРяЕФЙЬЬхМгШШЪБЃЌЪдЙмПкТдЯђЯТЧуаБЃЌдвђЪЧЪВУД?
ЁОВЮПМД№АИЁП
ИјЪдЙмРяЕФЙЬЬхМгШШЪБЃЌЪдЙмПкТдЯђЯТЧуаБЃЌФПЕФЪЧЗРжЙЪдЙмЯђЩЯЧуаБЪБгаЫЎЩњГЩЃЌЩњГЩЕФЫЎеєЦјРфФ§БфГЩаЁЫЎжщЃЌЗДСїЕНЪдЙмЕзВПЃЌЪЙЪдЙмЮТЖШОчСвБфЛЏЖјЦЦСбЁЃ
2.ФуБОНкПЮЕФНЬбЇжиФбЕуЪЧЪВУД?ФуЪЧШчКЮЪЕЯжЕФ?
БОНкПЮЮвЕФНЬбЇжиФбЕуЪЧЙЬЬхвЉЦЗЕФШЁгУетвЛЪЕбщВйзїЁЃдкНЬбЇЙ§ГЬжаЮЊСЫЭЛГіжиЕуЁЂЭЛЦЦФбЕуЃЌОпЬхЮвЪЧетбљРДзіЕФЃКЪзЯШЩЯПЮПЊЪМЃЌЯШШУбЇЩњУЧЛиЙЫжЎЧАбЇЯАЕФЪЕбщАВШЋддђЁЂвЧЦїЕШЃЌЮЊНгЯТРДЕФЪЕбщВйзїЕьЖЈЛљДЁЁЃНгЯТРДШУбЇЩњДјзХЮЪЬтШЅЙлВьЖрУНЬхжаЕФбнЪОЪЕбщЃЌЪІЩњНјаазмНсВйзїЕФВНжшЃЌВЂНјааЯргІЕФАхЪщЃЌжЎКѓЮвЛсдйДЮНјааВйзїЕФбнЪОЁЃзюКѓбЇЩњдкзджїВйзїЕФЙ§ГЬжаЃЌЮвЛсНјаабВЪгжИЕМЃЌМАЪБЗЂЯжВЂОРе§бЇЩњЕФДэЮѓЁЃ
2018ФъЯТАыФъНЬЪІзЪИёУцЪд-ЛЏбЇбЇПЦ-ЪдНВМАД№Бч-ПМЬтНтЮі
ГѕжаЛЏбЇЁЖдзгЕФЙЙГЩЁЗ
вЛЁЂПМЬтЛиЙЫ
 ЖўЁЂПМЬтНтЮі
ЖўЁЂПМЬтНтЮі
ЁОНЬбЇЙ§ГЬЁП
(вЛ)аТПЮЕМШы
ЁОЬсГіЮЪЬтЁП1897ФъЃЌгЂЙњПЦбЇМвЬРФЗЩЗЂЯжСЫДјИКЕчЕФЕчзгЃЌШЫРрНвПЊСЫдзгФкВПНсЙЙЕФУиУмЁЃдзггЩФФаЉВПЗжЙЙГЩФи?
ЁОбЇЩњЛиД№ЁПдзгКЫКЭКЫЭтЕчзгЁЃ
ЁОЬсГіЮЪЬтЁПДѓМвЖМжЊЕРЕчзгЪЧДјИКЕчЕФЃЌФЧУДдзгЯдЪВУДЕчадФи?НгЯТРДЮвУЧбЇЯАСЫдзгЕФКЫЕчКЩЪ§гыКЫЭтЕчзгЪ§ЕФЙиЯЕКѓОЭгаД№АИСЫЁЃ
(Жў)ЬНОПаТжЊ
ЁОЖЏЛбнЪОЁПдзггЩЮЛгкдзгжааФЕФдзгКЫКЭКЫЭтЕчзгзщГЩЕФЃЌетаЉЕчзгШЦзХдзгКЫЕФжааФдЫЖЏЃЌОЭЯёЬЋбєЯЕЕФаааЧШЦзХЬЋбєдЫаавЛбљЁЃЭЌбЇУЧПЩвдПДЖЏЛФЃФтбнЪОЁЃ
ЁОЬсГіЮЪЬтЁПдзгКЫгжгЩЪВУДЮЂСЃЙЙГЩФи?
ЁОбЇЩњЛиД№ЁПжЪзгКЭжазгЁЃ
ЁОНЬЪІНВНтЁПУПИіжЪзгДј1ИіЕЅЮЛЕФе§ЕчКЩЃЌжазгВЛДјЕчЃЌЖјУПИіЕчзгДј1ИіЕЅЮЛЕФИКЕчКЩЁЃ
ЁОЬсГіЮЪЬтЁПИљОнБэ3-1жаМИжждзгЕФЙЙГЩЃЌаЁзщЬжТлЃЌЮвУЧПЩвдЕУГіЪВУДНсЙћ?
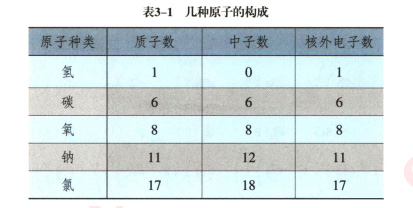
ЁОбЇЩњЛиД№ЁПжЪзгЪ§ЕШгкКЫЭтЕчзгЪ§;дзгФкВПе§ЁЂИКЕчКЩЪ§ФПЯрЕШЁЃ
ЁОНЬЪІзмНсЁПдзгКЫФкжЪзгЫљДјЕчКЩгыКЫЭтЕчзгЕФЕчКЩЪ§СПЯрЕШЃЌЕчадЯрЗДЃЌвђДЫЃЌдзгВЛЯдЕчадЁЃдзгКЫЫљДјЕФе§ЕчКЩЪ§ЃЌМДКЫЕчКЩЪ§ЃЌЕШгкКЫФкжЪзгЪ§ЃЌвВЕШгкКЫЭтЕчзгЕФЪ§ФПЁЃ
МДЃККЫЕчКЩЪ§=жЪзгЪ§=КЫЭтЕчзгЪ§ЁЃ
(Ш§)ЭиеЙЬсЩ§
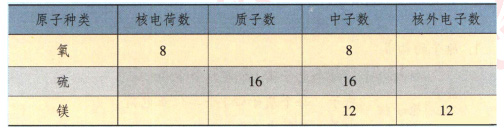
ЁОЬсГіЮЪЬтЁПЬюаДЯТБэжаЕФПеИёЁЃ
(ЫФ)аЁНсзївЕ
аЁНсЃКв§ЕМбЇЩњзмНсБОНкПЮЕФФкШнЁЃ
зївЕЃКдЄЯАКЫЭтЕчзгЕФХХВМЗНЪНЁЃ
ЁОАхЪщЩшМЦЁП

ЁОД№БчЬтФПНтЮіЁП
1.жЪСПЪ§гыЯрЖддзгжЪСПЕФЧјБ№?
ЁОВЮПМД№АИЁП
ЭЌжждЊЫиЕФжЪзгЪ§ЯрЭЌЃЌЖјжазгЪ§ПЩФмВЛЭЌЃЌМДДцдкЖржжКЫЫиЁЃЖјжЪСПЪ§жИЕФЪЧКЫЫижажЪзгЪ§гыжазгЪ§ЕФКЭЃЌЯрЭЌдЊЫиЕФВЛЭЌКЫЫиЕФжЪСПЪ§ВЛЭЌЁЃ
ЯрЖддзгжЪСПЮЊИїКЫЫиЕФЦНОљЯрЖджЪСПЁЃЭЌжждЊЫиЕФЯрЖддзгжЪСПжЛгавЛИіЪ§жЕЁЃ
2.ФуетНкПЮЕФжиЕуЪЧЪВУД?ФуЪЧдѕбљГЪЯжЕФ?
ЁОВЮПМД№АИЁП
КЫЕчКЩЪ§гыКЫЭтЕчзгЪ§ЕФЙиЯЕЃККЫЕчКЩЪ§=жЪзгЪ§=КЫЭтЕчзгЪ§ЁЃ
ЭЈЙ§аЁзщЬжТлЕФаЮЪНЃЌШУЭЌбЇУЧИљОнБэжаМИжждзгЕФЙЙГЩжаИїСЃзгЕФЕчКЩЪ§ФПЙиЯЕЃЌдкНЬЪІв§ЕМЯТЗжЮіЬжТлЕУГіНсЙћЁЃ
РДдДЃКбЇдБЗжЯэ
 ЮЂаХ
ЮЂаХ ЮЂВЉ
ЮЂВЉ QQбЇЯАШК
QQбЇЯАШК

 ЕиЪаЗжаЃЃК
ЕиЪаЗжаЃЃК ЗўЮёЕчЛАЃК029-85568912
ЗўЮёЕчЛАЃК029-85568912