2018ФъЯТАыФъНЬЪІзЪИёУцЪд_ИпжаЛЏбЇ_ЪдНВМАД№БчЃЈЕквЛХњЃЉ
ЗЂВМЪБМфЃК2019-04-12 11:23:31 БрМЉЃКЪІДѓДДГЬНЬг§
вЛЁЂПМЬтЛиЙЫ
ЬтФПРДдДЃК1дТ5ШеЩЯЮч КўФЯЪЁдРбєУцЪдПМЬт
ЪдНВЬтФПЃК
1.ЬтФПЃКЮяжЪЕФСП
2.ФкШнЃК
дкбаОПЮяжЪзЊЛЏЕФЙ§ГЬжаЃЌШЫУЧГ§СЫЙизЂЮяжЪзЊЛЏЗНЗЈЕФбЁдёЁЂзЊЛЏЬѕМўЕФПижЦвдЭтЃЌЛЙЪЎЗжЙизЂзЊЛЏЙ§ГЬжаЮяжЪМфЕФЖЈСПЙиЯЕЁЃ
гЩгкЛЏбЇБфЛЏжаЩцМАЕФдзгЁЂЗжзгЛђРызгЕШЕЅИіСЃзгЕФжЪСПЖМКмаЁЃЌФбвджБНгНјааГЦСПЃЌЖјЪЕМЪВЮМгЗДгІЕФСЃзгЪ§ФПЭљЭљКмДѓЃЌЮЊСЫНЋвЛЖЈЪ§ФПЕФЮЂЙлСЃзггыПЩГЦСПЮяжЪжЎМфСЊЯЕЦ№РДЃЌдкЛЏбЇЩЯЬив§ШыЮяжЪЕФСП(amount of substance)ЁЃ
ЮяжЪЕФСПЪЧЙњМЪЕЅЮЛжЦжаЕФЛљБОЮяРэСПжЎвЛЃЌЗћКХЮЊnЃЌЕЅЮЛЮЊФІЖћ(МђГЦЮЊФІЃЌЗћКХЮЊmol)ЁЃ1 molФГжжЮЂСЃМЏКЯЬхжаЫљКЌЕФЮЂСЃЪ§гы0.012 kg C-12жаЫљКЌЕФдзгЪ§ЯрЭЌЁЃ0.012 kg C-12жаЫљКЌЕФдзгЪ§ГЦЮЊАЂЗќйЄЕТТоГЃЪ§ЁЃгУNAБэЪОЁЃАЂЗќйЄЕТТоГЃЪ§NAНќЫЦЮЊ6.02×10ЕФ23mol-1ЁЃР§ШчЃК
1 mol O2жадМКЌ6.02×10ЕФ23ИібѕЗжзг;
1 mol CжадМКЌ6.02×10ЕФ23ИіЬМдзг;
1 mol H2SO4жадМКЌ6.02×10ЕФ23ИіСђЫсЗжзг;
1 mol NaOHжадМКЌ6.02×10ЕФ23ИіNa+КЭ6.02×10ЕФ23ИіCl-;
n mol ФГжжЮЂСЃМЏКЯЬхжаЫљКЌЮЂСЃЪ§дМЮЊn×6.02×10ЕФ23ЁЃ
ЮяжЪЕФСП(n)ЁЂАЂЗќйЄЕТТоГЃЪ§(NA)КЭЮЂСЃЪ§(N)жЎМфДцдкШчЯТЙиЯЕЃК
N=n×NA
3.ЛљБОвЊЧѓЃК
(1)МђвЊаДГіНЬбЇЙ§ГЬЁЃ
(2)НЬбЇЙ§ГЬжавЊгаЪЪЕБЕФЬсЮЪЛЗНкЁЃ
(3)вЊЧѓХфКЯНЬбЇФкШнгаЪЪЕБАхЪщЩшМЦЁЃ
(4)ЪдНВЪБМфЪЎЗжжгЁЃ
Д№БчЬтФП1.ЬсИпПЮЬУНЬбЇгааЇадЕФЗНЗЈКЭВпТдЪЧЪВУД?
2.ФІЖћЪЧЮяжЪЕФжЪСПЕЅЮЛЁЃетжжЫЕЗЈЖдТ№?
ЖўЁЂПМЬтНтЮі
ЁОНЬбЇЙ§ГЬЁП
(вЛ)ИДЯАОЩжЊ ЕМШыаТПЮ
ЬсЮЪбЇЩњЛЏбЇЗДгІЕФБОжЪЃЌбЇЩњЛиД№жЎКѓЬсГіМйЩшЃКвЊЪЧПЩвдМЦЫуЗДгІга“ЖрЩй”СЃзгВЮМгЗДгІЃЌЮвУЧЪЧВЛЪЧПЩвдПижЦЗДгІФи?ЪЧЗёПЩЖЈСПЕФвЊЧѓЖрЩйСЃзгВЮМгЗДгІ?в§ЗЂбЇЩњЫМПМКЭЬжТлЁЃ
НЬЪІНсКЯбЇЩњЬжТлФкШнНјааЙщФЩКЭзмНсЃКЮЂЙлСЃзгЃЌИњЧАУцР§згжаЕФДѓУзЁЂТЬЖЙЕШЃЌдкМЦСПБОжЪЩЯЪЧвЛбљЕФЃЌВЛПЩФмЭЈЙ§Ъ§Ъ§ФПЃЌЕУЕНОпЬхЕФЖрЩйЁЃЬсГіаТЮЪЬтЃКГЦСПСЃзгжЪСППЩвдТ№?ФЧЮвУЧвЊдѕУДАьФи?в§ШыБОНкПЮЁЖЮяжЪЕФСПЁЗЁЃ
(Жў)ЧщОАЩшжУ аТПЮНВЪк
1.ЮяжЪЕФСП
НЬЪІНВНтЮяжЪЕФСПетвЛЮяРэСПЕФИХФюЁЂЕЅЮЛКЭЗћКХЁЃЫЕУїЮяжЪЕФСПЪЧЙњМЪЦпИіЛљБОЮяРэСПжЎвЛЁЃ
2.АЂЗќйЄЕТТоГЃЪ§
ЬсЮЪЃКЭЌбљЪЧЮяРэСПЃЌБШШчжЪСПЃЌШЫУЧЙцЖЈКУвЛЯЕСаБъзМЪЧЖржиЃЌБШШч1 gЁЂ10 gЕШЃЌФЧУДЃЌЦфЫћЪТЮяЕФжЪСПОЭИњЩшСЂКУЕФБъзМШЅЖдееЃЌОЭПЩвдЕУГіЪєгкЫћздМКЕФжЪСПЁЃЭЌбљЕФЮяжЪЕФСПвВгаздМКЕФБъзМЁЃ
НЬЪІНјааНВНтЃКЪЙгУЮяжЪЕФСПЃЌвЊЩшСЂ1 molЪЧЖрЩйЁЃЖјетИіЖрЩйЃЌОЭЪЧАЂЗќйЄЕТТоГЃЪ§ЁЃЫќЕФЗћКХЪЧNAЃЌНќЫЦЮЊ6.02×10ЕФ23 mol-1ЁЃгаСЫетИіИХФюЃЌШЮКЮЪ§ФПЕФЮЂЙлСЃзгЖМПЩвдгУЮяжЪЕФСПРДБэЪОЃЌЭЌбљЃЌШЮвтЕФСЃзгЪ§ФПвВПЩвдгУЮяжЪЕФСПРДБэЪОЁЃ
ЬсЮЪЃК1 mol O2ЁЂH2ЁЂNaClжаКЌгаЮЂЙлСЃзгЪ§ФПЮЊЖрЩйЃЌn mol ФГжжЮЂСЃМЏКЯЬхжаЫљКЌЮЂСЃЪ§дМЮЊЖрЩйЁЃбЇЩњЫМПМВЂЛиД№ЃЌНЬЪІНјаазмНсЃКЮяжЪЕФСП(n)ЁЂАЂЗќйЄЕТТоГЃЪ§(NA)КЭЮЂСЃЪ§(N)жЎМфДцдкШчЯТЙиЯЕЃКN=n×NA
(Ш§)ЭиеЙЬсЩ§ аЁНсзївЕ
аЁНсЃКзмНсБОНкПЮбЇЕНЕФФкШнЃЌЪеЛёСЫФФаЉЁЃ
зївЕЃКВщевАЂЗќйЄЕТТоетЮЛПЦбЇМвЕФМђНщЁЃ
ЁОАхЪщЩшМЦЁП
ЮяжЪЕФСП
1.ЮяжЪЕФСП(n)ЃКЕЅЮЛЪЧmolЁЃ
2.АЂЗќйЄЕТТоГЃЪ§(NA)ЃКN=n×NA
ЁОД№БчЬтФПНтЮіЁП
1.ЬсИпПЮЬУНЬбЇгааЇадЕФЗНЗЈКЭВпТдЪЧЪВУД?
ЁОВЮПМД№АИЁП
ЬсИпПЮЬУНЬбЇгааЇадЕФЗНЗЈКЭВпТдЃК(1)ДгШЯЪЖЗЂеЙЕФЪгНЧНјаабЇЩњЗжЮі;(2)ЩюШыЗжЮіНЬбЇФкШн;(3)ЬсЩ§дЫгУИїжжНЬбЇММФмЕФФмСІЁЃ
2.ФІЖћЪЧЮяжЪЕФжЪСПЕЅЮЛЁЃетжжЫЕЗЈЖдТ№?
ЁОВЮПМД№АИЁП
етИіЫЕЗЈЪЧДэЮѓЕФЃЌФІЖћЪЧЮяжЪЕФСПЕФЕЅЮЛЃЌЮяжЪЕФСПЪЧвЛИіЮяРэСПЕФУћГЦ;ЫќЪЧБэЪОЙЙГЩЮяжЪЕФЛљБОЮЂСЃЪ§ФПЖрЩйЕФвЛИіЮяРэСП;ЙњМЪЩЯФІЖћетИіЕЅЮЛЪЧвд0.012kg12CжаЫљКЌЕФдзгЪ§ФПЮЊБъзМЕФЃЌМД1molСЃзгМЏЬхЫљКЌЕФСЃзгЪ§гы0.012kg12CжаЫљКЌЕФдзгЪ§ЯрЭЌЃЌдМЮЊ6.02×10ЕФ23ИіЁЃ
ИпжаЛЏбЇЁЖеєСѓЁЗ
вЛЁЂПМЬтЛиЙЫ
ЬтФПРДдДЃК1дТ5ШеЩЯЮч ЫФДЈГЩЖМУцЪдПМЬт
ЪдНВЬтФПЃК
1.ЬтФПЃКеєСѓ
2.ФкШнЃК
ДгЛьКЯЮяжаЗжРыКЭЬсДПФГаЉЮяжЪЃЌГ§СЫПЩгУЙ§ТЫЁЂеєЗЂЕШЗНЗЈЭтЃЌЖдгквКЬЌЛьКЯЮяЃЌЛЙПЩвдРћгУЛьКЯЮяжаИїзщЗжЕФЗаЕуВЛЭЌЃЌгУеєСѓЕФЗНЗЈГ§ШЅвзЛгЗЂЁЂФбЛгЗЂЛђВЛЛгЗЂЕФдгжЪЁЃ
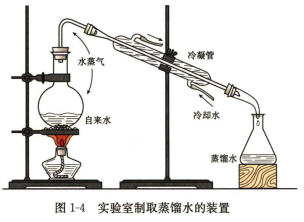
Р§ШчЃЌЪЕбщЪвЭЈЙ§еєСѓЕФЗНЗЈГ§ШЅздРДЫЎжаКЌгаЕФCl-ЕШдгжЪжЦШЁеєСѓЫЎЁЃЪЕбщЪвжЦШЁеєСѓЫЎГЃгУЕФзАжУШчЭМ1-4ЫљЪОЁЃ


(1)НЬбЇЙ§ГЬжавЊЩшжУаЁзщЬжТлЁЂЛЅЖЏЛЗНкЁЃ
(2)ШчЙћашвЊЪЕбщЛђИЈжњНЬбЇЙЄОпЃЌВЩгУгябдФЃФтМДПЩЁЃ
(3)вЊЧѓХфКЯНЬбЇФкШнгаЪЪЕБАхЪщЩшМЦЁЃ
Д№БчЬтФПЃК
1.МђЪіЫЎЕФеєСѓЪЕбщжагУЕНЕФвЧЦїЩшБИ?
2.НЬбЇЙ§ГЬжаЖдгкбнЪОЪЕбщгаЪВУДвЊЧѓ?
ЖўЁЂПМЬтНтЮі
ЁОНЬбЇЙ§ГЬЁП
(вЛ)ЕМШыаТПЮ
ЁОЬсГіЮЪЬтЁПдкКЃБпЃЌгцУёУЧЖМЪЧдѕУДНтОіЩњЛюгУЫЎЕФЮЪЬтЕФФи?ШчКЮАббЮЫЎБфЮЊЕЫЎФи?ЮвУЧНёЬьОЭРДАяжњгцУёУЧНтОіетИіЮЪЬтЁЃ
(Жў)аТПЮНВЪк
ЁОЬсГіЮЪЬтЁПвћгУЕФздРДЫЎЪЧДПОЛЕФЫЎТ№?
ЁОбЇЩњЛиД№ЁПВЛЪЧЃЌздРДЫЎжаГ§СЫКЌгаCl-ЃЌЛЙКЌгаКмЖрЮДГ§ШЅЕФПЩШмаддгжЪЁЃ
ЁОЬсГіЮЪЬтЁПдѕбљМьбщздРДЫЎжаКЌгаCl-?
ЁОбЇЩњЛиД№ЁППЩвдЯђздРДЫЎжаМгШыЯѕЫсЫсЛЏЕФЯѕЫсвјШмвКЃЌЙлВьЕНгаУїЯдЕФАзЩЋГСЕэЩњГЩЁЃжЄУїздРДЫЎжаШЗЪЕКЌгаТШРызгЁЃ
ЁОЬсГіЮЪЬтЁПгУЪВУДЗНЗЈГ§ШЅздРДЫЎжаЕФТШРызгФи?ФмЗёМгШыЯѕЫсвјШмвК?
ЁОбЇЩњЛиД№ЁПВЛФмЃЌЛсв§ШыаТЕФдгжЪЁЃ
ЁОНЬЪІв§ЕМЁПСЊЯЕдкМвРяЩеПЊЫЎЕФЪБКђЃЌЙјИЧЩЯГЃгаЫЎжщГіЯжЃЌетаЉЫЎжщЪЧЪВУД?етМўЪТЖдФугаЪВУДЦєЗЂ?
ЁОаЁзщЬжТлЁПЙјИЧЩЯЕФЫЎжщЪЧДПОЛЕФЫЎЃЌЮЊСЫЕУЕНДПОЛЕФЫЎЃЌПЩвдЯШНЋЫЎМгШШБфЮЊЫЎеєЦјЃЌЪеМЏРфФ§КѓЕФЫЎеєЦјЁЃ
ЁОЬсГіЮЪЬтЁПдѕбљШЗШЯЮвУЧЕУЕНЕФвКЬхОЭЪЧДПОЛЕФеєСѓЫЎ?
ЁОбЇЩњЛиД№ЁПЯђЦфжаМгШыЯѕЫсвјШмвКМьбщШмвКжаЪЧЗёЛЙДцдкCl-ЁЃ
ЁОЪгЦЕеЙЪОЁПЪЕбщЪвжЦШЁеєСѓЫЎЕФеєСѓзАжУМАеєСѓЙ§ГЬЁЃ
ЁОЬсГіЮЪЬтЁПЙлПДЪгЦЕЃЌЫМПМеєСѓОРњСЫФФСНИіЙ§ГЬЃЌИїВПЗжзАжУЕФзїгУЪЧЪВУД?
ЁОЪІЩњЙВЭЌзмНсЁПеєСѓЪЧеєЗЂКЭРфФ§СНжжВйзїЕФСЊКЯЃЌдкетРяЩеЦПЃКЭЈЙ§МгШШАбЫЎБфГЩЫЎеєЦј;РфФ§ЙмЃКРфФ§ЫЎеєЦјжиаТБфЮЊвКЬЌЫЎ;ХЃНЧЙмЁЂзЖаЮЦПЃКАбРфФ§ЫЎЕМШызЖаЮЦПжаЁЃ
ЁОЬсГіЮЪЬтЁПеєСѓдРэЪЧЪВУД?
ЁОбЇЩњЛиД№ЁПРћгУвКЬЌЛьКЯЮяжаИїзщЗжЗаЕуВЛЭЌЃЌгУеєСѓЕФЗНЗЈГ§ШЅвзЛгЗЂЁЂФбЛгЗЂЛђВЛЛгЗЂЕФЮяжЪЃЌдйРфФ§вдЗжРыећИізщЗжЕФВйзїЙ§ГЬЁЃ
ЁОЬсГіЮЪЬтЁПРфШДЫЎЕФЭЈШыЗНЯђЮЊЪВУДвЊзёбЯТНјЩЯГі?
ЁОбЇЩњЛиД№ЁПЮЊСЫЪЙеєСѓГіЕФЫЎеєЦјгыРфШДЫЎГЄЪБМфГфЗжНгДЅЃЌдіДѓРфФ§ЫЎгыеєЦјЕФНгДЅУцЛ§ЃЌЪЙРфШДЫЎДјзпИќЖрШШСПЃЌШШНЛЛЛаЇТЪБШНЯИпЃЌЗНБуЫЎеєЦјЕФРфФ§ЁЃ
ЁОЬсГіЮЪЬтЁПеєСѓЙ§ГЬжаЛЙашвЊзЂвтФФаЉЮЪЬт?
ЁОаЁзщзмНсЁПЩеЦПвЊЕцЩЯЪЏУоЭјМгШШВЛФмжБНгИјЩеЦПМгШШ;ЩеЦПФквКЬхЕФЬхЛ§ВЛФмГЌЙ§ЩеЦПШнЛ§ЕФ2/3;ЩеЦПжавЊМгШыЗаЪЏЗРжЙБЌЗа;ЪЕбщПЊЪМЪБЃЌЯШПЊРфФ§ЫЎКѓМгШШЃЌНсЪјЪБЃЌЯШЭЃжЙМгШШКѓЙиРфФ§ЫЎ;ШмвКВЛПЩеєИЩЁЃ
(Ш§)ЙЎЙЬЬсИп
ЁОНЬЪІв§ЕМЁПИїЪЕбщаЁзщИљОнетвЛзАжУжЦШЁеєСѓЫЎЃЌВЂМьбщТШРызгДцдкгыЗёЁЃ
(бЇЩњНјааеєСѓЪЕбщЃЌВЂМьбщТШРызгЃЌНЬЪІбВЛижИЕМЁЃ)
ЁОбЇЩњЪЕбщЁПНЬЪІбВЛижИЕМЃЌЦРМлзмНсбЇЩњЪЕбщВйзїЁЃ
(ЫФ)аЁНсзївЕ
аЁНсЃКНЬЪІгыбЇЩњЙВЭЌзмНсЁЃ
зївЕЃКЫМПМЛьКЯвКЬхжаШєКЌгаЖржжзщЗжЃЌШчКЮЭЈЙ§еєСѓзАжУЗжБ№ЕУЕНИїИізщЗжЃЌЫљгУзАжУгыБОНкПЮЫљбЇгаКЮВЛЭЌЃЌВЂЫбМЏЕЛЏКЃЫЎЕФЦфЫћЗНЗЈЁЃ
ЁОАхЪщЩшМЦЁП
еєСѓ
1.зАжУЃКЩеЦП→РфФ§Йм→ХЃНЧЙм→зЖаЮЦП
2.дРэЃКИїЮяжЪЗаЕуВЛЭЌ
3.зЂвтЪТЯюЃК
ЁОД№БчЬтФПНтЮіЁП
1.МђЪіЫЎЕФеєСѓЪЕбщжагУЕНЕФвЧЦїЩшБИ?
ЁОВЮПМД№АИЁП
ЬњМмЬЈЁЂОЦОЋЕЦЁЂЪЏУоЭјЁЂеєСѓЩеЦПЁЂРфФ§ЙмЁЂЮТЖШМЦЁЂНКШћЁЂХЃНЧЙм(ЮВНгЙм)ЁЂзЖаЮЦПЁЂНКЙмЁЃ
2.НЬбЇЙ§ГЬжаЖдгкбнЪОЪЕбщгаЪВУДвЊЧѓ?
ЁОВЮПМД№АИЁП
ЖдгкНЬбЇЙ§ГЬжаЃЌНЬЪІНјаабнЪОЪЕбщгавдЯТЛљБОвЊЧѓЃКЂйУїШЗЪЕбщЕФФПЕФ;ЂкОЁПЩФмБЃжЄЪЕбщЕФГЩЙІ;ЂлШЗБЃЪЕбщАВШЋЁЂЛЗБЃЁЂЮоЮлШО;ЂмзЂвтЪЕбщВйзїЕФЙцЗЖад;ЂнБпЪОЗЖБпЯђбЇЩњНВНт;ЂоОЁСПЬсИпЖдгкбЇЩњЕФПЩМћЖШЁЃ
ЩЯвЛЦЊЃК2018ЯТАыФъГѕжаЛЏбЇНЬЪІзЪИёжЄУцЪдПМЬтЃЈОЋбЁЃЉЕкЫФХњ
ЯТвЛЦЊЃКзюКѓвЛвГ
 ЮЂаХ
ЮЂаХ ЮЂВЉ
ЮЂВЉ QQбЇЯАШК
QQбЇЯАШК

 ЕиЪаЗжаЃЃК
ЕиЪаЗжаЃЃК ЗўЮёЕчЛАЃК029-85568912
ЗўЮёЕчЛАЃК029-85568912